EUA aprovam tratamento com transfusões de plasma para pacientes com coronavírus
Primeiros estudos apontam que 35% dos doentes se recuperam após receber o tratamento
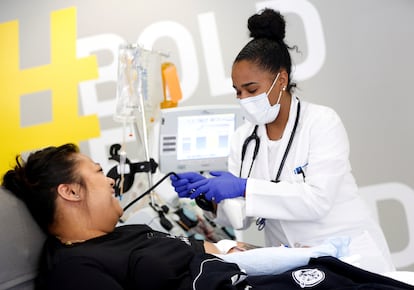

A Administração de Alimentos e Medicamentos dos Estados Unidos (FDA, na sigla em inglês) autorizou o uso emergencial de plasma como tratamento para pacientes com coronavírus. A agência federal analisou nos últimos meses os resultados de doentes que receberam transfusões do componente líquido do sangue de pacientes que se recuperaram da doença. O plasma contém um alto nível de anticorpos que, segundo as análises da agência, ajudam na recuperação dos pacientes em alguns casos.
A agência tinha interrompido o processo na semana passada, alegando que os resultados das pesquisas não tinham sido conclusivos. Neste domingo, a FDA anunciou ter analisado os resultados de 20.000 pacientes que receberam transfusões de plasma – todos com menos de 80 anos, hospitalizados, mas sem necessidade de respirador artificial. A agência afirmou que pelo menos 35% dos doentes tiveram uma recuperação favorável após receber o tratamento. Nos Estados Unidos, estima-se que 70.000 pessoas com a covid-19 já tenham recebido uma transfusão de plasma de um paciente recuperado.
A mudança de rumo deste domingo é repentina e radical. “Os estudos realizados neste ano mostram que o plasma dos pacientes que se recuperaram da covid-19 têm o potencial de ajudar a tratar pacientes que estão sofrendo os efeitos deste terrível vírus”, afirmou Stephen Hahn, diretor da agência. Os estudos sobre o tratamento ainda estão em andamento, e o órgão se comprometeu a atualizar sua autorização conforme avançarem.
Até agora, o único tratamento autorizado pela FDA era o antiviral experimental remdesivir, elaborado pelo laboratório Gilead, e que recebeu sinal verde nos Estados Unidos em maio. O medicamento foi criado para tratar o ebola e a hepatite, mas não deu resultados satisfatórios. Contra a covid-19, o fármaco atua como um bloqueador do vírus quando entra no corpo humano. Até agora, os Estados Unidos registaram 5,6 milhões de casos e 176.000 mortos pela doença.
A nova autorização foi anunciada neste domingo pelo próprio presidente Donald Trump na Casa Branca. Nesta semana, no Twitter, ele tinha atacado a FDA por supostamente impedir que a vacina contra o coronavírus estivesse disponível para os norte-americanos antes de 3 de novembro, data das eleições presidenciais. “A FDA está dificultando muito que as companhias farmacêuticas cheguem às pessoas para fazer os testes com as vacinas”, escreveu Trump. Sob pressão do presidente, a agência cedeu.
Informações sobre o coronavírus:
- Clique para seguir a cobertura em tempo real, minuto a minuto, da crise da Covid-19;
- O mapa do coronavírus no Brasil e no mundo: assim crescem os casos dia a dia, país por país;
- O que fazer para se proteger? Perguntas e respostas sobre o coronavírus;
- Guia para viver com uma pessoa infectada pelo coronavírus;
- Clique para assinar a newsletter e seguir a cobertura diária.